Félelmetes szuperbaktériumok támadnak az emberekre
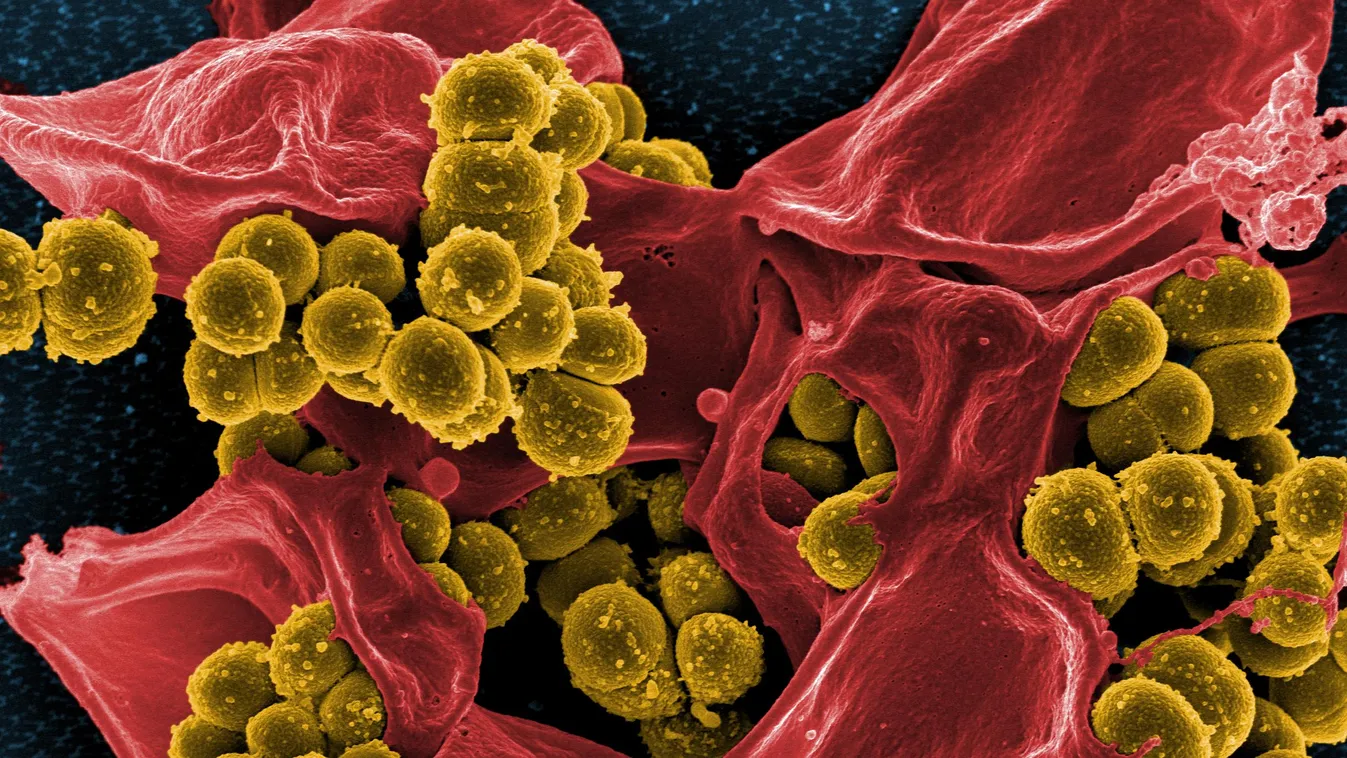

A mikrobiális „sötét anyagból" – eddig tenyészthetetlen, ezért alig ismert baktériumokból – izolált új, erőteljes antibiotikum, a klovibaktin (clovibactin) mindenféle kártékony baktériummal, köztük az eddigi antibiotikumoknak ellenálló szuperbaktériumokkal is megbirkózik – állítja az anyagot előállító és tesztelő nemzetközi kutatócsoport. Az Utrechti Egyetem (Hollandia), a Bonni Egyetem (Németország), a Német Fertőzéskutató Központ (DZIF), a Northeastern University of Boston (USA), valamint a NovoBiotic Pharmaceuticals gyógyszeripari startup (Cambridge, USA) kutatói által a Cell folyóiratban megjelentetett közlemény arról számol be, hogy a klovibaktin szokatlan mechanizmus útján öli meg a baktériumokat, amellyel szemben várhatólag nehezen vagy nem is alakulhat ki rezisztencia. A cikk leírja a klovibaktin felfedezésének menetét, és ismerteti a molekula sajátos ölőmechanizmusát.
A kórokozók antimikrobiális szerekkel szembeni rezisztenciája világszerte óriási egészségügyi problémát jelent, ezért mindenütt aktívan keresik a lehetséges új megoldásokat.
Sürgősen szükségünk van új antibiotikumokra azok ellen a baktériumok ellen, amelyek egyre inkább érzéketlenné válnak a mai klinikumban alkalmazott szerek többségével szemben"
– hangsúlyozta Markus Weingarth, az Utrechti Egyetem vegyészeti tanszékének kutatója. Az új antibiotikumok felfedezése azonban, úgy tűnik, nem triviális feladat: az utóbbi évtizedekben alig néhány új vegyület jelent meg a klinikumban, és ezek is jobbára a régebbi, ismert antibiotikumok újragondolásai.
„A klovibaktin más – szögezi le Weingarth. –
Mivel olyan baktériumokból izoláltuk, amelyeket korábban nem tudtunk laboratóriumban tenyészteni, a kórokozó baktériumok még nem találkoztak ilyen antibiotikummal, ezért nem is volt idejük arra, hogy rezisztenciát alakítsanak ki vele szemben."
A klovibaktin felfedezése egy kis USA-beli gyógyszeripari startuphoz, a NovoBiotic Pharmaceuticals-hoz, illetve Kim Lewishoz, a bostoni Northwestern University mikrobiológus professzorához fűződik. A professzor és a cég csapata korábban kifejlesztettek egy eszközt az annakelőtte tenyészthetetlennek vélt – és ezért olykor „mikrobiális sötét anyag"-nak titulált – baktériumok növesztésére. Meglepőnek tűnhet, de az összes ismert baktérium mintegy 99 százaléka nem tenyészthető, vagyis korábban nem sikerült a laboratóriumi kitenyésztése, ezért eddig új antibiotikumok után sem lehetett kutatni a körükben. Az iCHip névre keresztelt új eszköz segítségével azonban az amerikai kutatóknak sikerült az E. terrae ssp. Caronina-t, egy észak-karolinai homokos talajból kinyert baktériumalfajt laboratóriumi növekedésre bírniuk, s ennek izolátumaiban fedezték fel a klovibaktint.
Az egyetemek és a cég által közösen publikált Cell-cikkben a NovoBiotic Pharmaceuticals munkatársai bemutatják, ahogy a klovibaktin sikeresen legyőzi a kórokozó baktériumok széles spektrumát, és eredményesen kezeli a többszörösen ellenálló Staphylococcus aureus-szuperbaktériummal fertőzött egereket.
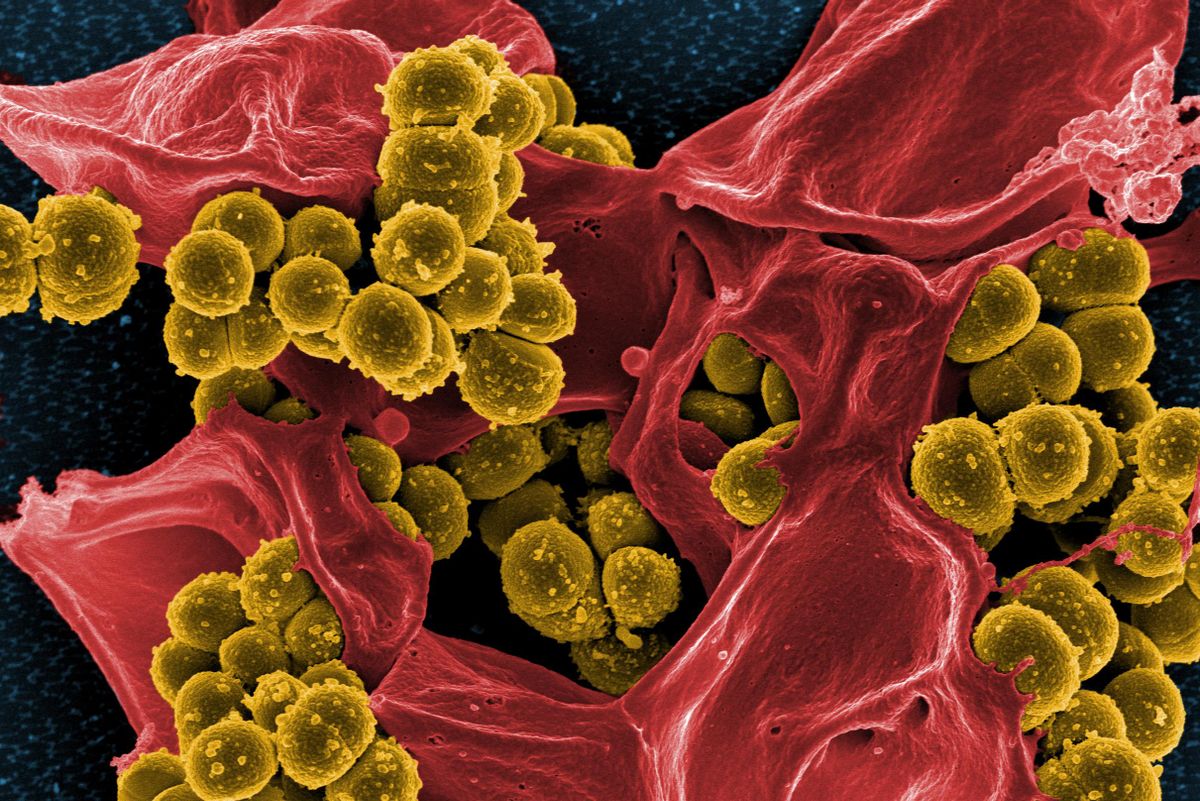
A klovibaktin szokatlan baktériumölő mechanizmussal bír.
Nem csupán egy, de rögtön egyszerre három olyan molekuláris építőanyagot támad, amelyek a baktériumot kívülről védő sejtfal felépítéséhez szükségesek.
E támadási pontok felderítése Tanja Schneiderhez és kutatócsoportjához köthető; Schneider, aki a Bonni Egyetem tanára és a közlemény egyik társszerzője, így magyarázta a lényeget: „A klovibaktin többcélpontú támadási mechanizmusa a bakteriális sejtfalszintézis több lépését egyidejűleg blokkolja. Ez fokozza a szer aktivitását, és lényegesen csökkenti a vele szembeni rezisztencia kialakulásának valószínűségét."
Annak részleteit, hogy a klovibaktin egész pontosan miként akadályozza a sejtfalszintézist, Markus Weingarth és csapata derítették fel az Utrechti Egyetemen. A szilárd fázisú NMR nevű speciális technikát alkalmazták, hogy a klovibaktin működését nagyjából olyan körülmények között tudják tanulmányozni, amilyenek a baktériumokban is fennállnak.
„A klovibaktin úgy fogja körbe a pirofoszfát-molekulát, mint egy szorosan markoló kesztyű. Vagy mint egy ketrec, amely foglyul ejti a tartalmát" – vázolja Weingarth, hozzátéve: innen ered a szer neve is, ugyanis a „klouvi" görögül ketrecet jelent. A klovibaktin mechanizmusa azért figyelemre méltó, mert csak ahhoz a változatlan pirofoszfát-molekularészlethez kötődik, amely a sejtfal-építőkövekben állandó, de a változékony cukor-részletekhez nem. „Mivel a klovibaktin csak a célmolekulák változatlan, megőrzött részletéhez kötődik, a baktériumoknak nagyon fel kell kötniük a gatyamadzagot, ha ellenállóvá akarnak válni vele szemben.
Vizsgálataink során egyetlen esetben sem tapasztaltuk a klovibaktinnal szembeni rezisztencia kialakulását"
– folytatta a kutató.
A klovibaktin valójában még ennél is többre képes. Amikor célpontjához köt, spontán hosszú szálakká szerelődik össze a baktériumok felszínén. Ezek a szálak tartósan stabilak maradnak, ami garantálja, hogy a célmolekulák egészen addig blokkolódnak, amíg az immunrendszer el nem pusztítja a baktériumot. „Mivel ezek a szálak csak a baktériumok sejtfelszínén alakulnak ki, az emberi sejtek sejthártyáján nem, a klovibaktin kizárólag a baktériumokat károsítja, miközben az emberi sejtekre nézve nem toxikus – fűzte hozzá végül Weingarth. – Ezért a klovibaktin kitűnő kiindulópont olyan hatóanyagok tervezéséhez, amelyek szelektíve megölik a bakteriális kórokozókat anélkül, hogy azok ellenállóvá válhatnának vele szemben."











