Ezek a legfontosabb tények a koronavírusokról
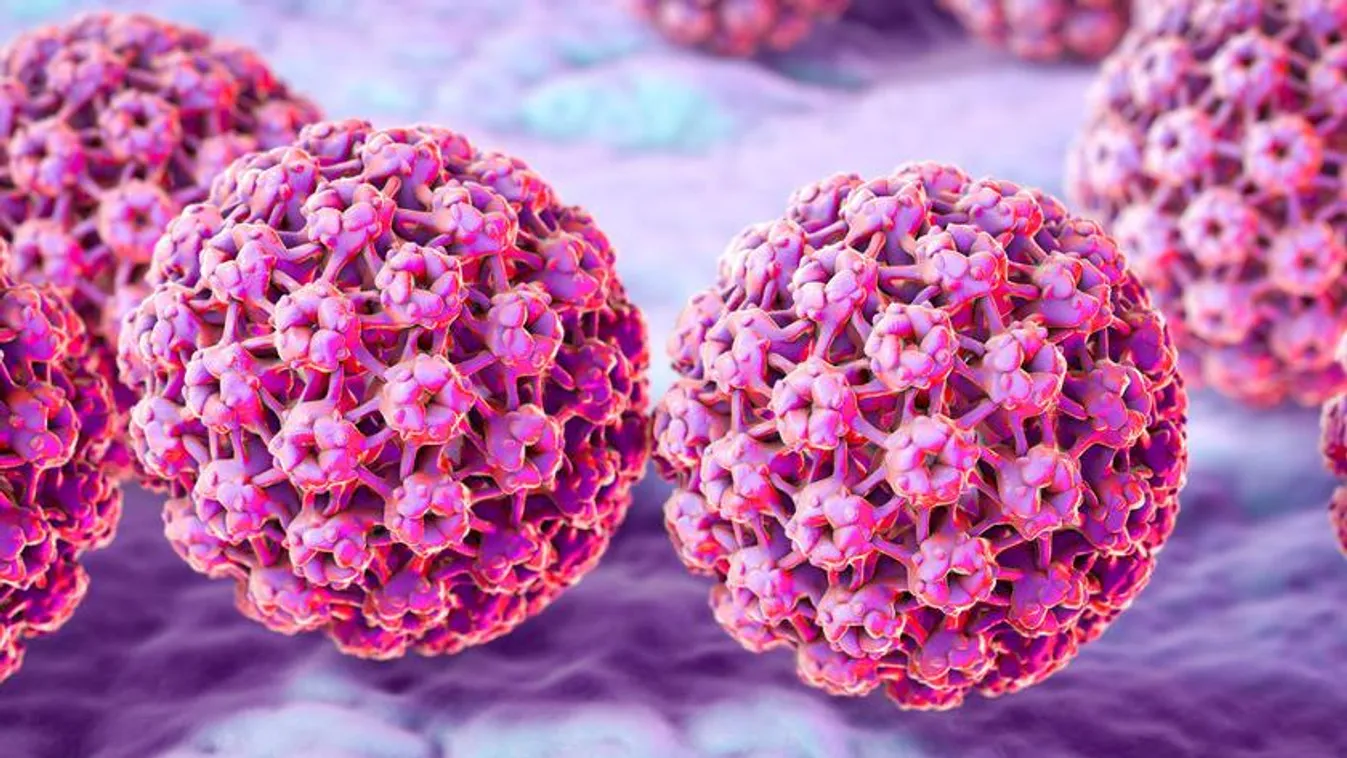

A vírus nem más, mint egy vagy néhány örökítőanyagdarabka, fehérjetokba – és esetenként egy sejthártyaszerű lipidburokba – csomagolva. Ezen túlmenően viszont ahány vírus, annyi féle.
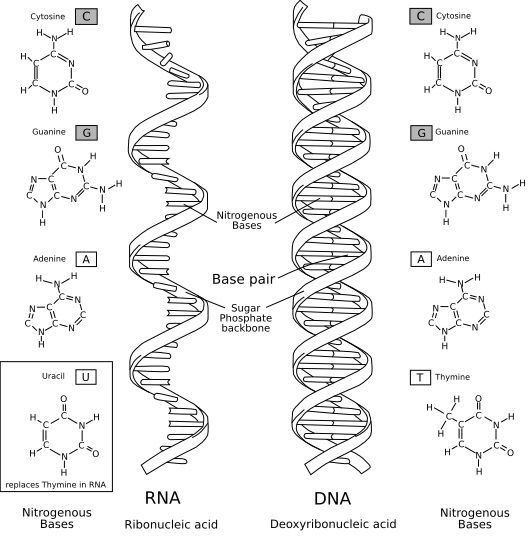
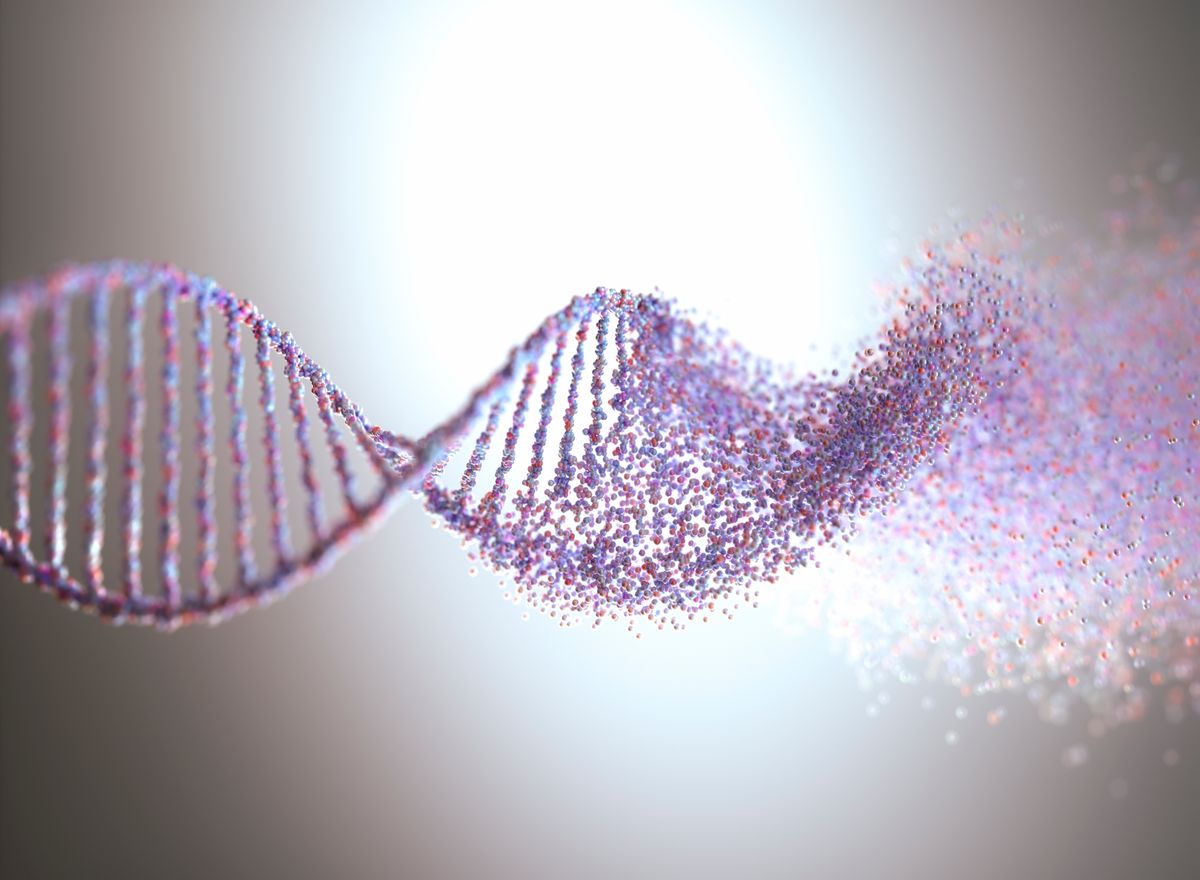
Míg a baktériumoktól az emberig az összes sejtes szervezetben a kétféle természetes nukleinsav, a dezoxiribonukleinsav (DNS) és a ribonukleinsav (RNS) közül mindig a DNS tölti be az örökítőanyag szerepét, méghozzá a két komplementer láncból összekapcsolódó kettősszálú formában,
a vírusok e téren jóval nagyobb változatosságot mutatnak:
örökítőanyaguk lehet akár a DNS, akár az RNS, s bármelyiknek az egyszálú vagy kétszálú formája.
A fehérjeburok ön-összeszerelő, vagyis további beavatkozás nélkül spontán összeáll az őt alkotó fehérjékből,
és szerveződhet a kinyújtott nukleinsavlánc körül csavarformában – ahogy az elsőként felfedezett vírus, a dohánymozaikvírus esetében –, alkothat szabályos téridomot, leginkább a húsz háromszög által határolt ikozaédert a felgombolyodott nukleinsav körül – ahogy az a legtöbb állati vírusra jellemző –, vagy lehet összetett, az előbbi elemekből és más járulékos szerkezetekből kombinálódó, ahogy azt a baktériumokat megtámadó bakteriofágok esetében láthatjuk.
Helyesebben: láthatnánk, ha a vírusok nem lennének annyira kicsik, hogy nemcsak szabad szemmel, de még hagyományos optikai mikroszkóppal sem figyelhetők meg.

A fénymikroszkóppal elvileg elérhető legnagyobb nagyítás kb. 1000-szeres, ezért 0.2 mikrométernél (200 nanométernél) kisebb részleteket nem tudunk vele kivenni.
Ez a legkisebb baktériumok mérettartománya; a vírusok azonban ennél akár 10-szer kisebbek,
csupán 20-30 nanométer átmérőjűek is lehetnek, ezért szerkezetük tanulmányozásához a 100 000-szeresnél is erősebb nagyítást lehetővé tevő elektronmikroszkópok szükségesek.

A mi legkisebb magvas sejtjeink, a nyiroksejtek nagyjából 12 mikrométeres átmérőjűek, így méretben úgy viszonyulnak egy 120 nanométeres HIV vírusrészecskéhez, mint egy fél méter átmérőjű strandlabda egy 5 mm átmérőjű borsszemhez.
Aki a fekete-fehér, igen-nem típusú válaszokat szereti, annak most sajnos csalódnia kell, mert a természet egyáltalán nem engedelmeskedik az ember skatulyázó hajlamának. Hogy a vírusokat élőlénynek tekintjük-e vagy sem,
az attól függ, hogyan definiáljuk az életet,
s ennek megvitatásához kissé messzebbről érdemes elindulnunk. A zseniálisan provokatív evolúcióbiológus, Richard Dawkins vetette fel először Az önző gén című munkájában, hogy az élet alapegysége tulajdonképpen nem a szervezet vagy az egyed, hanem az örökítőanyag funkcionális egysége, a gén.

Ebből a nézőpontból nézve nem génjeink szolgálják testünket abban, hogy az felnövekedjék és szaporodjék, hanem a testünk az, amely génjeink szolgálatában áll: testünk voltaképpen egy túlélőgép, amelyet génjeink szerveznek saját szaporításuk érdekében maguk köré.
A földi élet – s valószínűleg bármely élet – alapegysége a replikátor: egy olyan entitás, amely saját megkettőződését elősegíti.
A földi élet kezdeteikor az első replikátorok valószínűleg rövid RNS-molekulák lehettek, a nukleinsavak ugyanis tudvalevőleg – a komplementer bázispárosodás révén – képesek saját másolatukat létrehozni.

Ezek az RNS molekulák idővel csapatokba verődtek, más biomolekulákkal – a mai fehérjék elődjeivel – társultak, majd egy lipidhártya révén fizikailag is elhatárolódtak a külső közegtől. Így alakulhattak ki az első sejtek, amelyek növekedtek és osztódtak, s minden osztódás alkalmával átadták örökítőanyaguk egy-egy másolatát utódjaiknak.
Mindazonáltal a nukleinsav köré épült sejt nem egyéb, mint a nukleinsav szolgálóleánya: működését az örökítőanyagban hordozott információ határozza meg, létének célja és értelme pedig az örökítőanyag másolásának elősegítése.
Attól a pillanattól fogva, hogy a saját örökítőanyaguk replikálásán szorgoskodó sejtek megjelentek az élet színpadán,
a nukleinsavak számára az önmásolás újabb lehetőségei nyíltak meg.
Bármely darabka nukleinsav felmondhatta a „társadalmi szerződést", s egy sejten belül elkezdhetett sokasodni az örökítőanyag többi részének rovására, hiszen ehhez a sejtben minden építőanyag és segédeszköz a rendelkezésre állt.
Ha ezt nem túl kapzsi módon tette, és nem lehetetlenítette el az örökítőanyag egészének megkettőzését,
sikeresen elszaporodhatott a sejt génállományán belül.
Hogy ez mennyire kifizetődő replikációs stratégia, azt ékesen bizonyítja, hogy az emberi genetikai állomány csaknem fele (úgy 44 százaléka) ilyen ún. transzpozábilis elemekből – a génállományon belül szaporodó-ugráló genetikai töredékekből – áll, amelyek vajmi keveset tesznek bele a nagy közösbe.
Innen már nem sok lépés az olyan önző genetikai elemek kialakulása, amelyek gazdasejtjükben elszaporodva nem visszaülnek a génállományba,
hanem szétrobbantják a sejtet, fehérjetokba csomagolódva szerterajzanak, és a szomszédos gazdasejtekbe jutva ugyanezt megismétlik.
Ez pedig pontosan az a mód, ahogyan a legtöbb vírus működik.
Ha az első replikátorok RNS-molekulák voltak, s őket tekintjük minden élet elődjének, megfoszthatjuk-e őket az élet attribútumától?
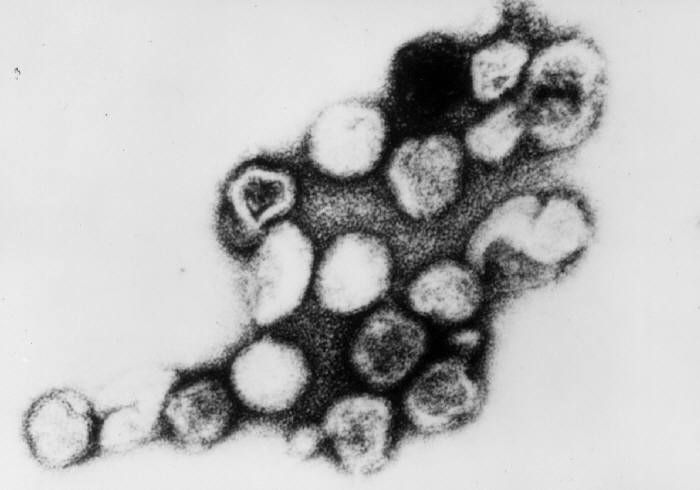
Másfelől viszont: ha élőnek tekintünk egy fehérjeburokba csomagolt nukleinsavdarabot, amely kizárólag egy élő – értsd: autonóm módon önmásoló – sejt segítségével tud szaporodni,
az olyan, mintha nem tennénk különbséget hardver és szoftver között.
Egy USB-meghajtón tárolt program a világűrben lebegve soha nem fog lefutni; ahhoz, hogy a program „életre keljen", be kell dugni a meghajtót egy számítógépbe, amely képes olvasni az eszközről és lefuttatni a kódot. A szoftver csak a hardver segítségével képes feltámadni; rajta kívül csupán nullák és egyesek sorozata. Akkor most egy vírus a gazdasejten kívül él vagy sem? A kérdést ki-ki a maga filozófiai ízlése szerint megválaszolhatja anélkül, hogy ez bármit is változtatna a dolgok természetén.
A vírusok származásának egyik lehetőségét a fentiekben már vázoltuk: legalábbis egy részük vélhetően egy néhai gazdasejt örökítőanyagából kiszakadt darabkát hordoz magában, rajta olyan génekkel, amelyek a vírusrészecske felépítéséhez és a gazdasejt átprogramozásához szükséges fehérjéket kódolják.
Egy másik hipotézis szerint a vírusok valaha önálló, sejtes szerveződésű élőlények voltak,
amelyek a parazita életmód hatására extrém módon leegyszerűsödtek. A megkérdőjelezhetetlenül élőlénynek tekintett baktériumok körében is akadnak kizárólag a gazdasejtjükön belül létezni tudó élősködők, amelyek egykori génjeik zömét elveszítették, hiszen ezekre immár semmi szükségük.
Hovatovább, fontos energiatermelő sejtszervecskéink, a mitokondriumok is autonóm baktériumok voltak valaha, ám úgy 1.45 milliárd évvel ezelőtt sejten belüli együttélő életmódra tértek át, s génállományuk az eltelt idő alatt a végletekig redukálódott,
azonban mindmáig van saját DNS-ük, és önállóan osztódnak sejtjeinken belül.
Egy harmadik elképzelés azt veti fel, hogy vírusok eredetét a sejtek előtti világban kell keresnünk, s ilyen értelemben a vírusszerű létmód magával a földi élettel egyidős.
A tudomány mindeddig egyik feltételezés mellett sem tette le egyértelműen a voksát, de két dolog bizonyos. Az egyik, hogy e hipotézisek nem kölcsönösen kizáróak. Mivel a máig leírt nagyjából 5000 vírusfaj – meg az a másik legalább millió, amit nem ismerünk – nem vezethető vissza egyetlen közös ősre,
a legvalószínűbb az, hogy a ma összefoglaló néven vírusnak nevezett legkülönfélébb furcsa szerzetek
az élet történetének más és más pontjain, más és más mechanizmus révén alakultak ki.
A másik bizonyos dolog az, hogy a vírusok története valóban a kezdetektől fogva összefonódik az élet mint olyan történetével.
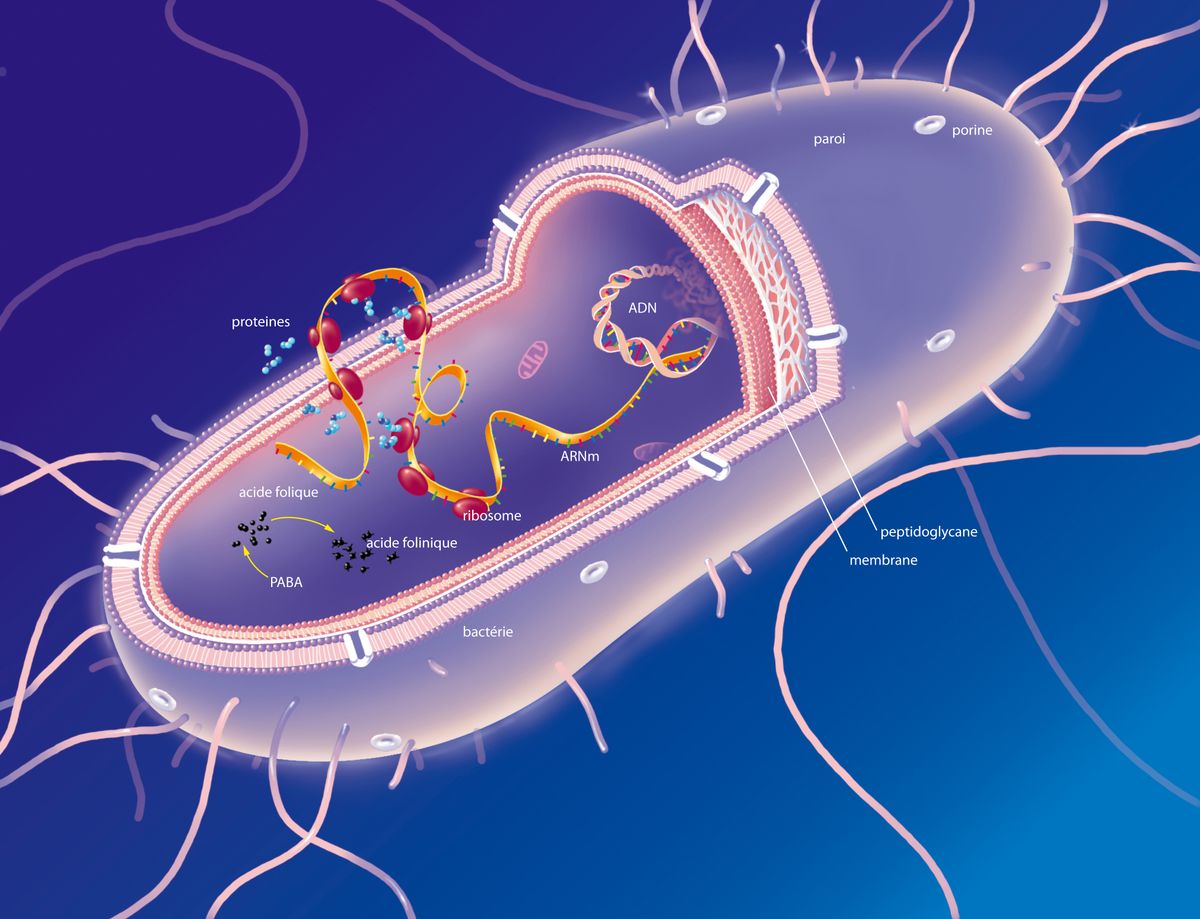
Valamennyi ismert sejtes létformának – az ősbaktériumoknak is hívott archaeáktól kezdve a „rendes" baktériumokon át a növényekig, gombákig és állatokig – megvannak a maguk vírusai, és az első vírusok már bizonyosan jelen voltak az élővilág történetének első nagy szétágazása, az archaeák és a baktériumok csoportjainak szétválása előtt.
Ami a miértet illeti, egy dolgot mindjárt le kell szögezni – észben tartva persze, hogy egy molekuláris gépezet esetében szándékokról szigorúan csak átvitt értelemben beszélhetünk –: nem szándékosan. Egy vírusnak egyáltalán nem célja vagy érdeke az, hogy a gazdáját megbetegítse, még kevésbé, hogy elpusztítsa,
hiszen szaporodása és terjedése a gazda életműködéseihez kötött.
A legjobb az a vírusnak, ha a gazdaszervezet él és virul, miközben a lehető legtovább és legnagyobb számban termeli és terjeszti a további vírusrészecskéket, amelyek így újabb gazdaszervezeteket tudnak megfertőzni.
Ezért aztán nagy evolúciós időskálán nézve a parazita-gazda kölcsönhatások tipikusan a békés együttélés felé haladnak;
a nagyon virulens és agresszív kórokozók rendszerint evolúciós értelemben újak, amelyeknek még nem volt idejük összecsiszolódni a gazdaszervezettel.
Az emberi szervezettel is számos teljesen ártalmatlan vírus él együtt, amelyek feltehetőleg igen ősi örökségeink; ilyenek például az anellovírusok vagy az adeno-asszociált vírusok. Éppen azért nem hallunk ezekről sokat – és sokszor felfedezésük is azért maradt le évtizedekkel a patogén vírusoké mögött –, mert semmi bajt nem okoznak.
Érthető módon nagyobb érdeklődés övezi azokat a vírusokat, amelyek valamilyen megbetegedést okoznak, és a vírusok jó része csakugyan ilyen. Noha – ahogy azt fentebb írtuk – egy ideális parazita elvileg életben hagyja gazdáját, a legtöbb vírus ténykedése a gyakorlatban mégiscsak a gazdasejt pusztulását vonja maga után.
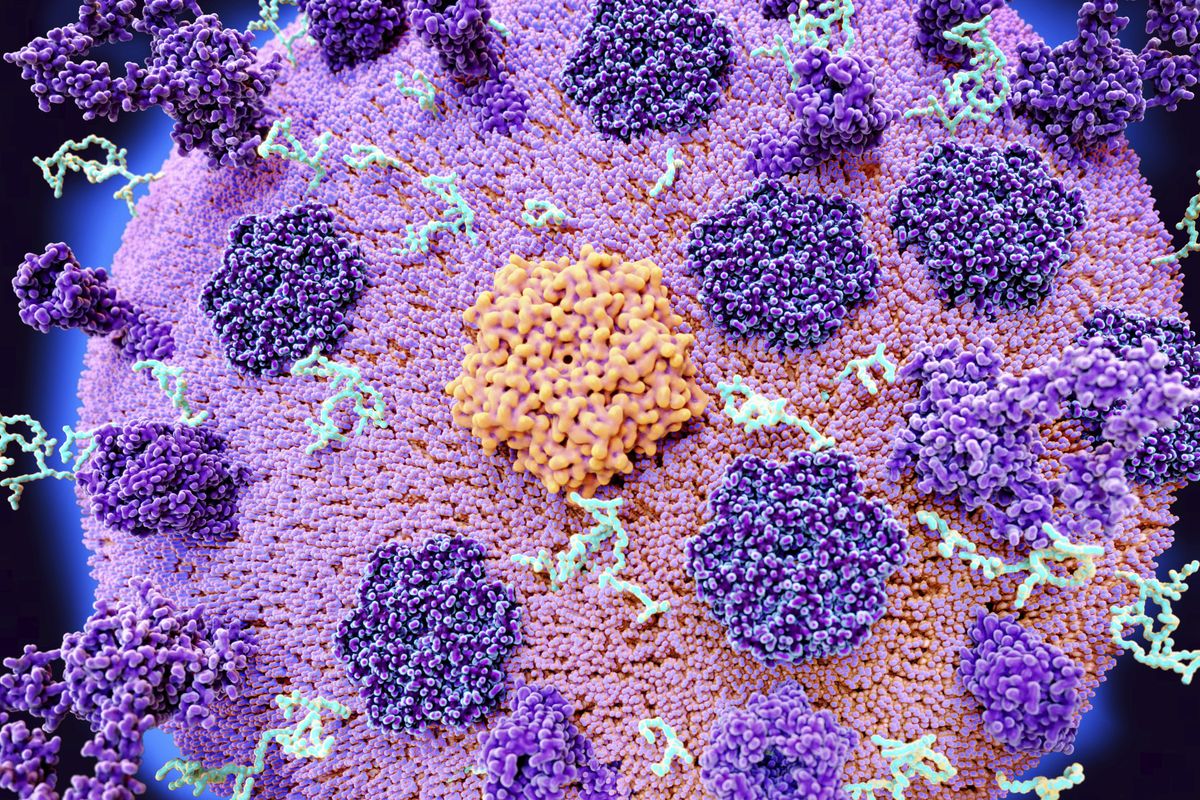
A vírus számára ez azért nem jelent zsákutcát,
mert a széteső gazdasejt a fertőzőképes vírusrészecskék sokaságát szórja szét,
s ezek a szervezeten belül hamar újabb élő áldozatokra találnak. Ahhoz, hogy a gazdasejt belehaljon a fertőzésbe, nem kell, hogy fizikailag szétrobbantsák a vírusrészecskék – bár ez is előfordulhat –; elég, ha a vírus a saját hatékony másolásának érdekében leállítja a sejt normális működéseit.
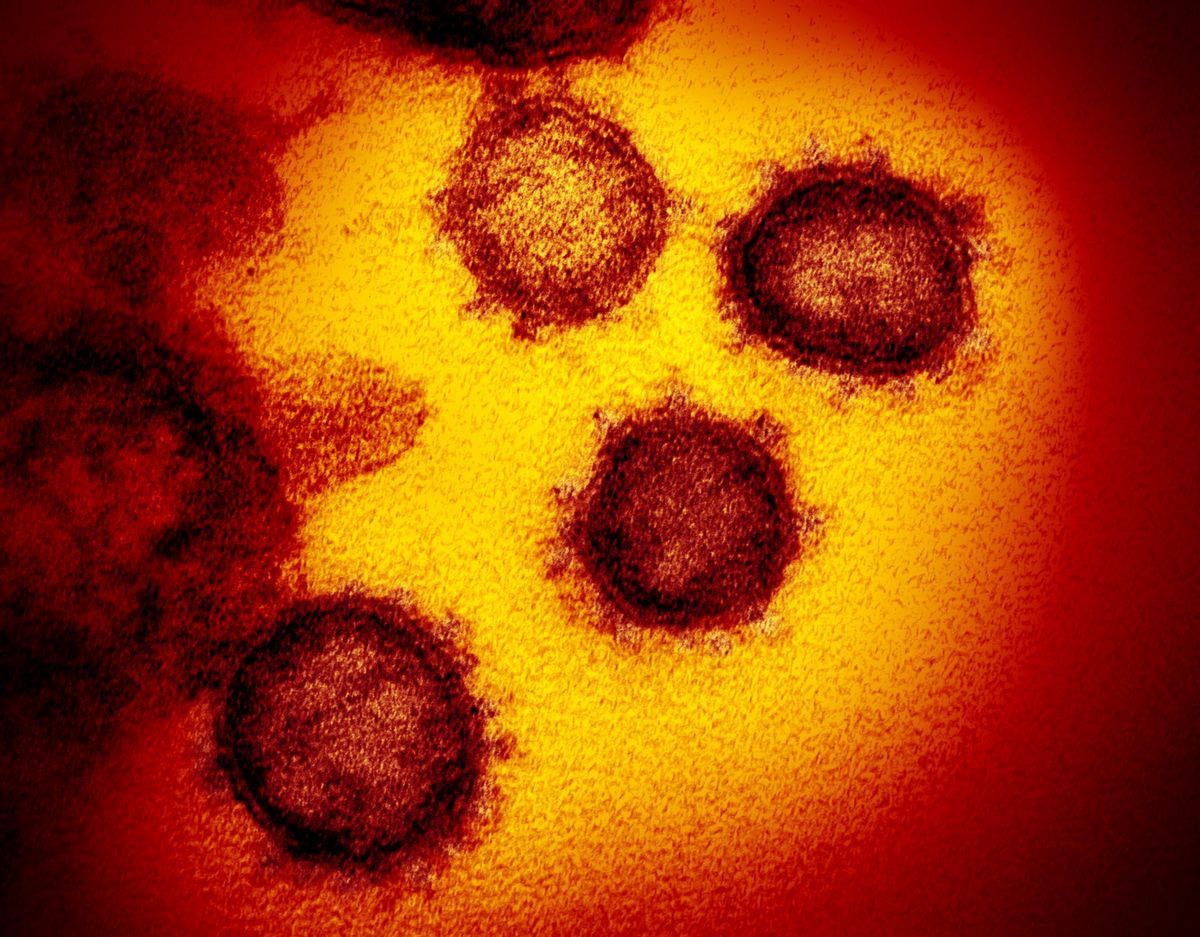
A leállással a sejt gyakran nem is a vírus támadó programját, hanem a saját védekező programját hajtja végre. A vírusok és gazdáik közötti több milliárd éves fegyverkezési versenyben a gazdák ellentámadásának egyik leghatékonyabb módja a „felperzselt föld" stratégiájának sajátos változata,
amely különösen a többsejtű szervezetek esetében nyer értelmet.
Bár működéseik leállításával az egyes gazdasejtek magukat is halálba taszítják, ezzel megakadályozzák a vírus szaporodását, így saját feláldozásuk árán megmenekíthetik a szervezet egészét.
Ezzel már előre is vetítettük azt, hogy az emberi szervezetben a vírusok okozta kár csak részint tulajdonítható a vírus szaporodása által közvetlenül előidézett sejthalálnak; legalább ilyen fontos, ha nem még fontosabb a sejt- és szervezet-szintű védekezés hozzájárulása.
A vírusfertőzött sejt nemcsak öngyilkosságot követhet el, hanem elpusztulhat azáltal is,
hogy az immunrendszer sejtjei – leginkább a sejtfelszínen óhatatlanul megjelenő víruseredetű fehérjetöredékeknek köszönhetően – lefülelik a benne zajló fertőzést, és szabályosan kivégzik, újfent a szervezet mint nagy egész védelmében.
A vírusfertőzés tünetei, vagyis azok a jelenségek, amelyeket mi betegségként észlelünk, főleg az immunrendszer vírusellenes fellépésével kapcsolatosak. A levertséget, rossz közérzetet jelmolekulák okozzák,
amelyeket a vírusok aktiválta immunsejtek bocsátanak a keringésbe.
Ezek biztosítják a hőközpontunk beállított hőmérsékletének feltekerését, vagyis a lázat, ugyanis a vírusok egy része nem képes magas hőmérsékleten replikálódni, egyúttal arra intik szervezetünket, hogy maradjon nyugalomban, és takarékoskodjék energiáival.
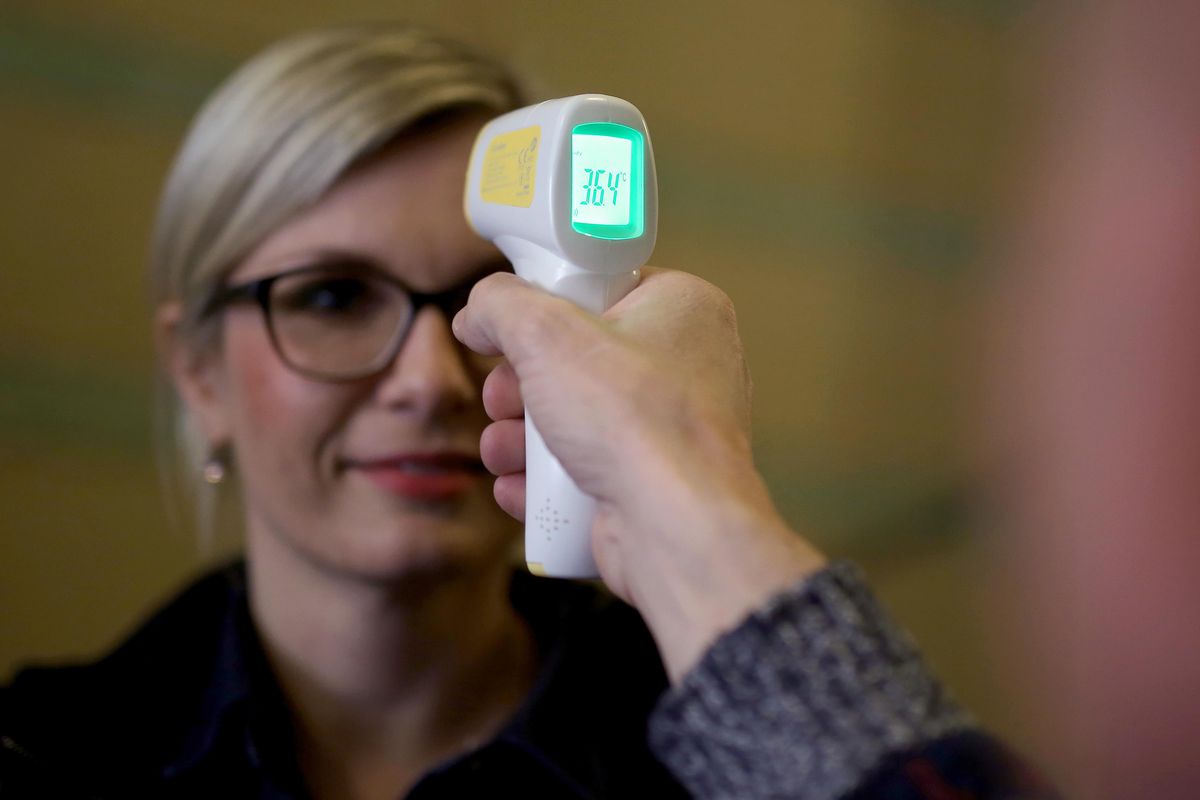
A fertőzött sejtek és az immunsejtek kölcsönhatása helyileg gyulladásos folyamatként jelenik meg,
annak minden velejárójával: fájdalommal és/vagy irritációval, illetve a fokozott véráramlás és a megnövekedett érfal-áteresztőképesség következményeivel, a duzzanattal és a szöveti folyadékgyülemmel.
Bár az immunválasz okozza a betegség kellemetlen, sőt, potenciálisan végzetes tüneteit, ez egyben a vírusfertőzés eliminálásának, a gyógyulásnak is a záloga.
Védekezés hiányában a vírus korlátlanul garázdálkodhat,
így szabályosan végigtarolja a rá fogékony sejtjeinket, ami nem csak potenciálisan, de majdnem biztosan halálhoz vezet.

Ilyesmi sajnos tényleg megesik csökkent immunvédelemmel rendelkező egyénekkel, például AIDS-betegekkel vagy szervátültetésen átesettekkel. Velük triviális vírusfertőzések is végezhetnek: az egészséges szervezetre veszélytelen citomegalovírus bennük végzetes tüdőgyulladást, a szintén jobbára ártalmatlan Epstein-Barr vírus heves lefolyású nyirokrákot okozhat.
Immunkompetens emberekben a vírusellenes immunválasz több fronton zajlik.
A vírusfertőzött sejtek felismerése és elpusztítása a sejtölő T-nyiroksejtek specialitása, amelyek közvetlen sejt-sejt kontaktus útján felfedezik a vírus-eredetű idegen fehérjetöredékeket, és halálra ítélik a fertőzött sejtet.
A B-nyiroksejtek ugyanakkor ellenanyagokat termelnek a vírus alkotórészeivel szemben, amelyek beborítják a vírusrészecskéket, így azokat nemcsak fertőzésképtelenné, de a falósejtek célpontjává is teszik.
S míg javában zajlik a harc, mind a T-, mind a B-nyiroksejtek egy része hosszú életű memóriasejtté alakul,
amely a kórokozóval való ismételt találkozás esetén azonnal és immár sokkal hatékonyabban tud támadásba lendülni.
Ez az immunológiai memória képezi a védőoltások biológiai alapját: a kórokozó jellegzetes motívumaival történő immunizálás felkészíti az immunrendszert a valódi ellenséggel való esetleges későbbi találkozásra.
És ugyanez az immunemlékezet az, amely a legtöbb kórokozó esetében megóv minket a többedik fertőződéskor a betegség újbóli kialakulásától.
Ha tehát az immunvédekezést teljesen elnyomnánk, hogy elkerüljük a kellemetlen vagy éppen veszélyes tüneteket,
azzal ellehetetlenítenénk a szervezet fellépését a vírussal szemben,
és az immunológiai emlékezet kialakulását is megakadályoznánk.
Napjainkban már hatékony antivirális szerekkel rendelkezünk például a herpeszvírusok okozta akut fertőzésekkel szemben, és egyes krónikus vírusfertőzéseket – köztük a HIV-et és a hepatitisz C-t – olyan gyógyszerekkel tudjuk kezelni,
amelyek évtizedekre, szerencsés esetben élethosszig lehetővé teszik a vírussal való többé-kevésbé tünetmentes együttélést.

Tény ugyanakkor, hogy az antivirális szerek jó része specifikus módon egy-egy meghatározott vírusra hat, míg az ún. széles spektrumú antibiotikumok – és a leggyakrabban felírt antibiotikumok ilyenek – jelzőjüknek megfelelően
a baktériumfajok sokaságával szemben hatékonyak.
Háziorvosunk ezért írhat fel nekünk elég nagy biztonsággal, pusztán tapasztalati alapon egy antibiotikumot anélkül, hogy tenyésztés útján megbizonyosodott volna az aktuális betegségünket okozó baktériumfaj rendszertani hovatartozásáról.
Ennek oka legalább részben a vírusok korábban emlegetett változatosságában keresendő. Bár a baktériumok is rendkívül sokfélék, nagy rendszertani csoportjaik rendelkeznek bizonyos egységes tulajdonságokkal, amelyek közös gyógyszer-támadáspontokat jelölnek ki.
Például a legtöbb baktérium sejtfallal védi magát, amely nélkül sokkal sérülékenyebb az immunrendszer támadásával szemben,
így a sejtfal felépítését gátló antibiotikumok – egyebek mellett a penicillin és származékai, vagy a cefalosporinok – rengeteg különböző sejtfalas baktérium ellen hatásosak.
Szintén általánosak (és a mienktől szerencsésen eltérőek) a baktériumok körében a fehérjegyártó apparátus alkotóelemei, ezért más antibiotikum-családok – például a makrolidok vagy a tetraciklinek – ezek célzásának köszönhetően alkalmazhatók széles körben.
A vírusok ezzel szemben nemigen rendelkeznek olyan átfogó közös sajátságokkal, amelyek értelmet adnának egy „mindenkire egy méret jó" típusú gyógyszeres támadásnak.
Tény, hogy a vírusok is rokonsági körökbe csoportosíthatók,
s egy-egy szer egy megadott körön belül általánosan alkalmazható lehet: jó példa erre a herpeszvírusok családjának több tagja, így a közönséges herpeszvírus, a bárányhimlővírus és a citomegalovírus ellen egyaránt (bár nem azonos mértékben) hatékony aciklovir.
Ám a különböző víruscsaládok oly távol eshetnek egymástól az örökítőanyag jellegét és az egész vírusrészecske szerkezetét, valamint a fertőzéshez és az örökítőanyag sokszorosításához használt fehérjekészletet illetően,
hogy esélytelen bennük közös támadáspontot találni.
Ez alól is akadnak persze kivételek: egymástól távol álló vírusok is használhatnak hasonló enzimeket például az örökítőanyaguk másolására vagy fehérjéik szabdalására, és e hasonlóságot kihasználva támadhatunk nemrokon vírusokat ugyanazzal a vegyülettel."
Elsősorban azért, mert a vírusok egy része hallatlanul gyorsan képes változni, márpedig a vakcináció csak akkor működik, ha a szóban forgó kórokozó nem ölt állandóan új alakot.
Egy folytonosan mutálódó vírus mozgó célpont:
hiába adjuk be oltásban az éppen aktuális változatát, ha jövőre, meg az azt követő évben már annyira megváltozik, hogy a memóriasejtek nem ismernek rá.
Egyes vírusokat a kötelező védőoltási kampányok a nemlét küszöbére tudtak szorítani. A polió, azaz a gyermekbénulás még az előző század derekán is tömeges pusztítást végzett,
de mára teljesen eltűnt a nyugati világból.
A mumpsz, a kanyaró (morbilli) és a rózsahimlő (rubeola) az 1960-as évek végén bevezetett kombinált MMR oltásnak köszönhetően a gyakori gyermekbetegségek sorából a szinte ismeretlenek közé került.
Az influenzának ezzel szemben minden szezonban más és más változatai támadnak,
és időnként felbukkannak olyan egészen újszerű törzsei, amelyek világméretű járványt okoznak.
Nyilvánvaló tehát, hogy egy gyermekkorban egyszer-kétszer beadott vakcina az influenzával szemben nem biztosíthat élethosszig tartó védettséget, mert a vírusnak eleve rengeteg változata köröz a világon, és állandóan újabbak állnak elő.
A vírusok változékonyságának két fő forrását érdemes megemlíteni. Az egyik az örökítőanyaguk másolásának pontatlansága, melynek folytán a mutációs rátájuk – a genomkettőződésenként bekövetkező másolási hibák hányada – a miénknél nagyságrendnyivel magasabb. Ha ehhez hozzávesszük a rendkívül rövid nemzedékváltási idejüket, érthetővé válik, hogyan tudhat egy vírusból hetek-hónapok alatt tucatnyi különböző variáns kialakulni.
Az új, és minden korábbitól drasztikusan eltérő vírustörzsek kialakulásának van egy ritkább, de annál látványosabb módja is:
ha két különböző vírus egyetlen gazdasejtben találkozik, és ott genetikai anyagot cserélnek, szakszóval: rekombinálódnak.
Ilyenkor egy olyan hibrid vírus áll elő, amely mindkét eredeti törzstől különbözik, ezért könnyen világhódító útra indulhat, mert egyetlen gazdaszervezet immunrendszere sem őriz róla emléket. A világjárványokat okozó vírusok rendszerint így állnak elő.
S bár annak az esélye, hogy két sikeresen rekombinálódni képes vírus pontosan ugyanazt a sejtet fertőzze meg, és a keveredés be is következzék, csillagászatian kicsi,
ne feledjük, hogy a próbálkozások száma viszont csillagászatian magas: egy felsőlégúti beteg egyetlen tüsszentéssel akár 200 millió vírusrészecskét is szétszórhat.
Hogy mégis lehetséges a szuperváltozékony vírusok, így az influenza ellen is olyan oltásokat kifejleszteni, amelyek legalábbis egy altípus legtöbb variánsával szemben védelmet nyújtanak, az két dolognak köszönhető.

Egyfelől ezeknek a vírusoknak is akadnak viszonylag állandó alkatrészeik, amelyek nem variálhatók tetszőlegesen, mert ha csak picit is változnak, már nem fognak működni. Másfelől az oltás kiváltotta immunválasz során nem csak pontosan a beadott vírusfehérjékkel,
hanem számtalan, azokra eléggé hasonlító fehérjével szemben is védetté válunk.
Így ha az oltást követően egy mutált, de nem a felismerhetetlenségig megváltozott változat fertőz meg minket, még mindig jó esélyünk van rá, hogy élvezhetjük a vakcina nyújtotta védettséget.
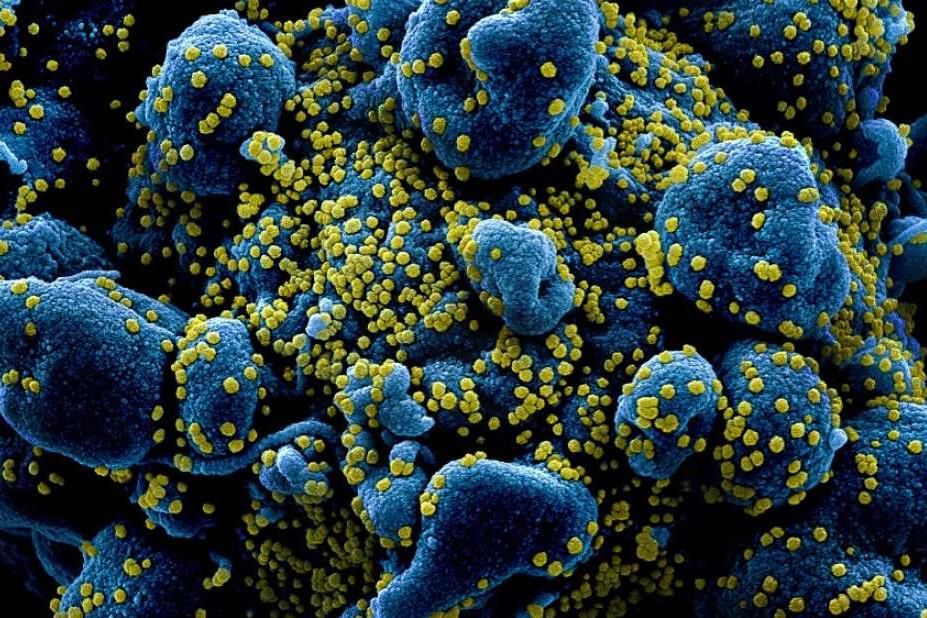
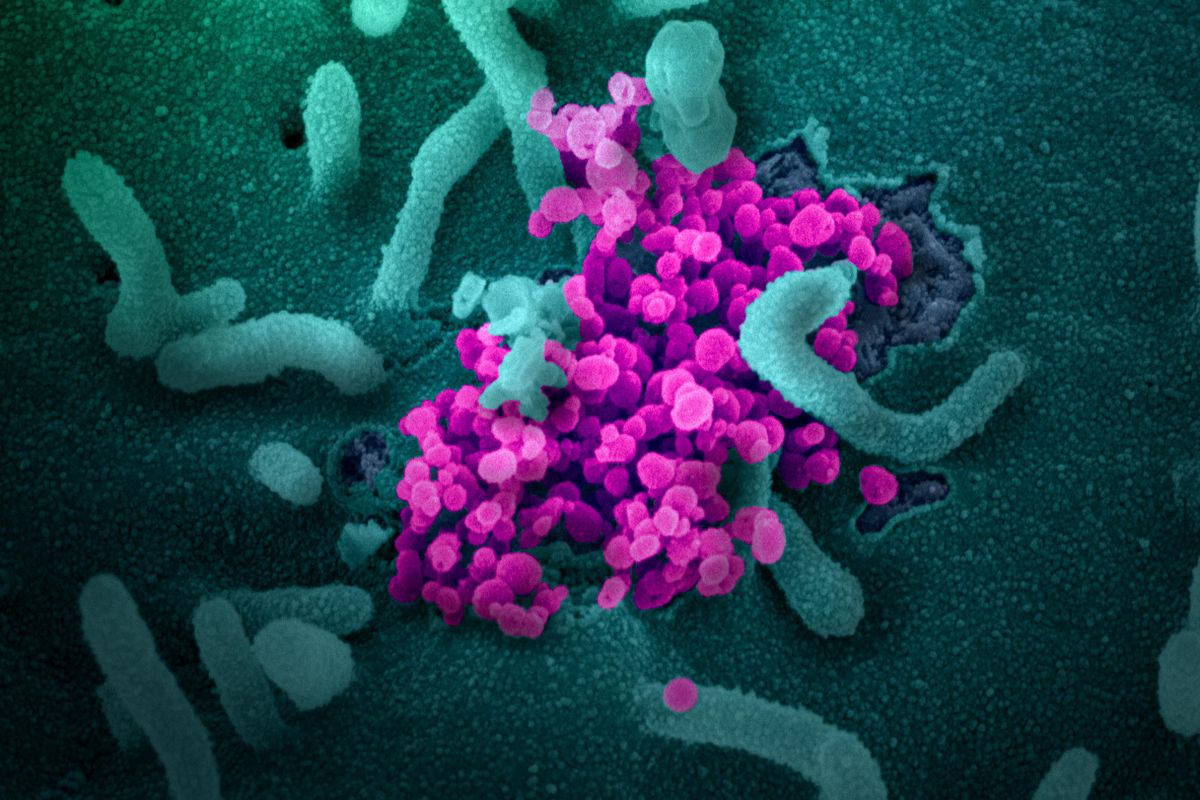
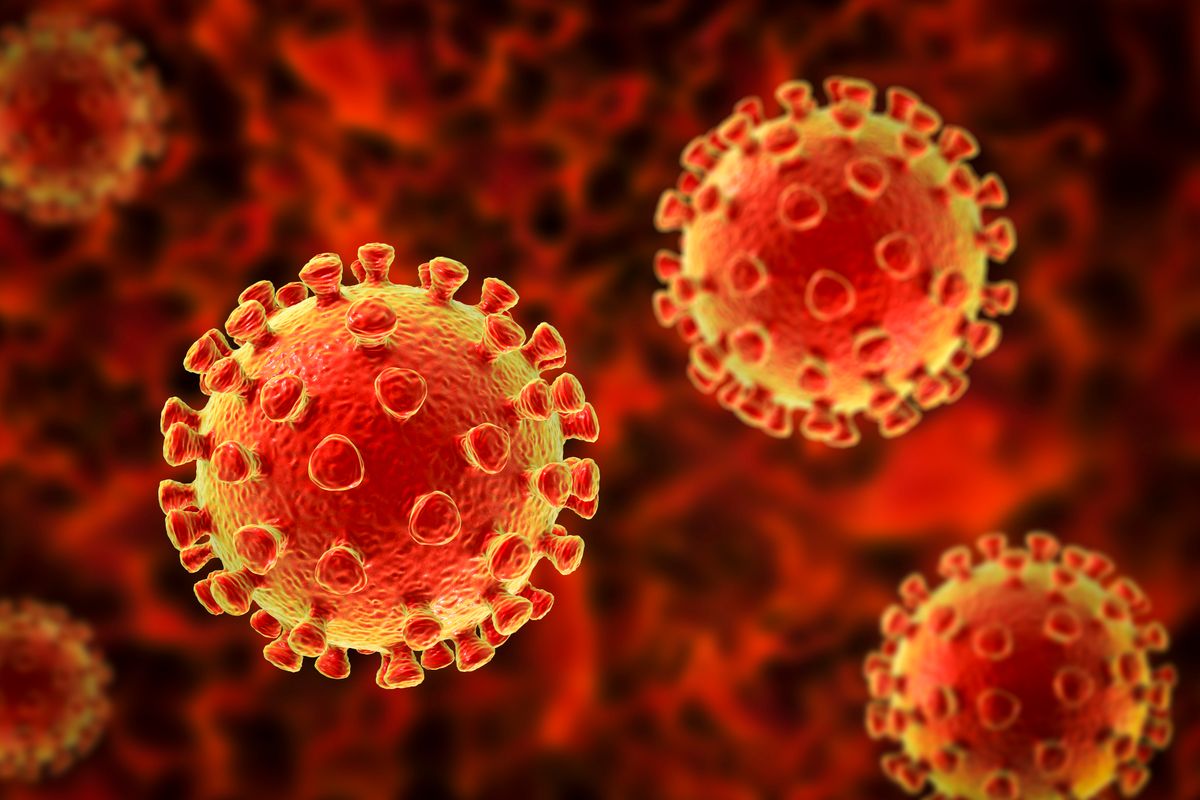
A COVID-19 vírusa a koronavírusok közé tartozik, több rokona emberben ártalmatlan légúti megbetegedést okoz, de a SARS és a MERS képében már volt alkalmunk veszedelmes koronavírusokkal is találkozni.
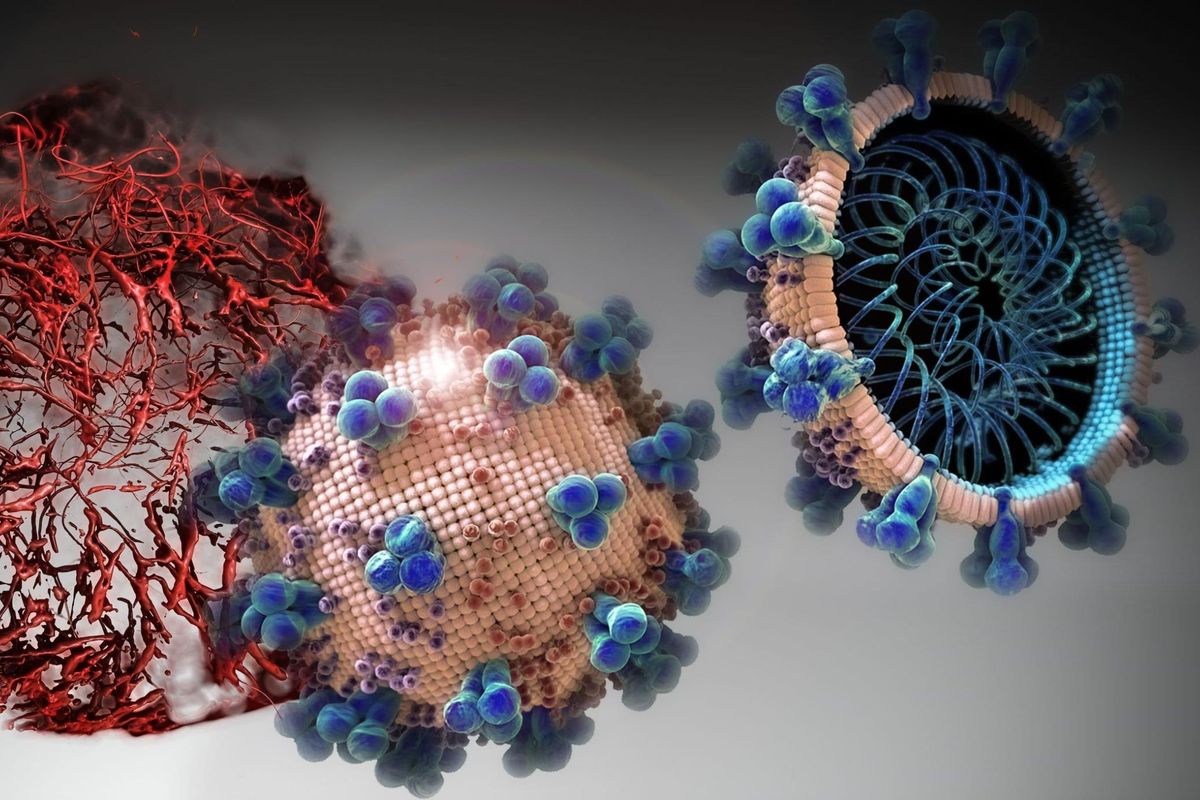
Örökítőanyaga egyszálú RNS, szerkezetére jellemző a fehérjetokot körülvevő lipidburok, amelyből a koronára emlékeztető, a gazdasejthez hozzákötődő tüskenyúlványok erednek.
A lipidburok érzékennyé teszi a detergensekre (pl. szappanra, mosószerre) és az alkoholos fertőtlenítőkre.
A koronavírus-részecskék átmérője megközelítőleg 125 nanométer, a mi legkisebb magvas sejtjeink átmérőjének századrésze (mint borsszem a strandlabdához képest).
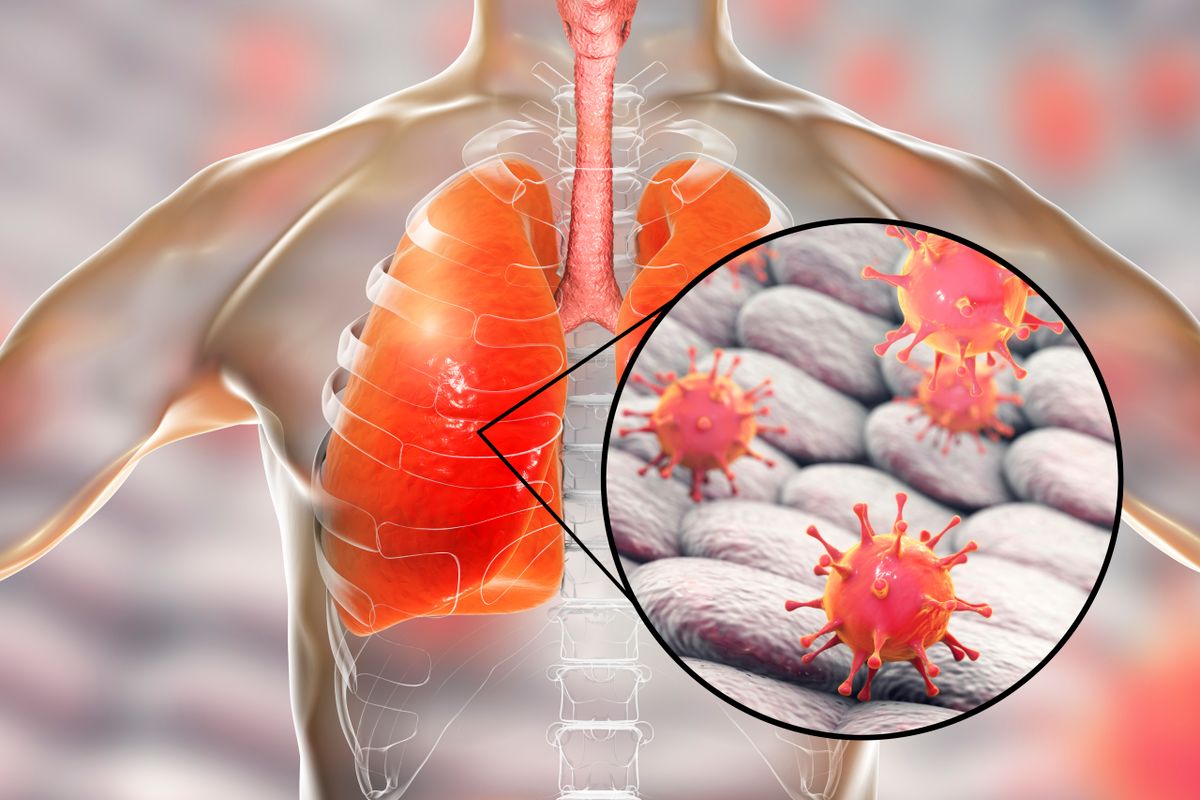
A COVID-19-re is igaz, hogy a betegséget a vírussal szembeni immunválasz teheti végzetessé. A COVID-19 a felső légutak és a tüdő hámját egyaránt képes megfertőzni. Amikor az immunrendszer a tüdő hámjában szaporodó vírust megtámadja, fokozódik a hajszálerekből az immunsejtek kilépése és a folyadékkiáramlás.
A folyadék felgyülemlik úgy a léghólyagocskák üregében, mint a léghólyagocskák és az őket körülvevő hajszálerek között, így egyszerre csökken a hatékony légzőfelület és romlik a légzési gázok cserélődése.
Az, hogy a fertőzöttek többsége tünetmentesen vagy enyhe tünetekkel vészeli át a betegséget, azt engedi gyanítani,
hogy a többi, relatíve ártalmatlan koronavírussal való korábbi találkozás ún. keresztvédettséget alakíthatott ki a COVID-19-cel szemben.
Vagyis hiába vadonatúj vírusról van szó, sokak immunrendszere számára mégis eléggé ismerősnek tűnik ahhoz a rokonokról őrzött régebbi emlékek alapján, hogy hamar és szinte észrevétlenül leküzdjék.
Ha ez a keresztvédettség csakugyan létezik és fontos szerepet játszik a tünetmentes fertőzöttekben, az reményt ad egy általánosan alkalmazható vakcina kifejlesztéséhez.
Mert bár a COVID-19 is igen változékony – a vírusnak máris számos genetikai variánsa kering –, ha az unokatestvéreivel való előzetes találkozás védelmet nyújthat ellene, akkor neki is biztosan akad olyan alkatrésze, amely kellően széles immunválaszt indukál.
Újabban felmerült a tuberkulózis elleni BCG oltás keresztvédő szerepe is a COVID-19-cel szemben. Ezzel kapcsolatban két kérdést kell megválaszolniuk a már szerveződő klinikai vizsgálatoknak. Az egyik, hogy az éppen COVID-19-cel megbetegedettek beoltása a BCG vakcinával enyhíti-e a betegség lefolyását az immunrendszer általános mozgósítása – főleg az ún. veleszületett, nemspecifikus immunválasz felpörgetése – révén.

A másik, ettől elvi szinten is eltérő kérdés, hogy élveznek-e bármi védettséget a COVID-19-cel szemben azok, akik a BCG védőoltást gyermekkorukban megkapták. Bizonyított, hogy a BCG oltás a tüdőgümőkór kórokozóján, a Mycobacterium tuberculosis-on kívül még számos patogén ellen védelmet nyújt a beadása utáni egy évben,
de hogy van-e ilyen élethosszig tartó ernyőhatása, és az érinti-e a COVID-19-et, az egyelőre tisztázandó.
Míg a COVID-19-specifikus vakcinára és antivirális szerekre várunk – és ez még akkor is legalább egy-másfél évig el fog tartani, ha minden szupergyorsan megy –, megpróbálhatunk már létező gyógyszereket „újrahasznosítani" a COVID-19 ellen.
A legkézenfekvőbbnek tűnik az antivirális szerek bevetése, de ahogy arra fentebb kitértünk, vírus és vírus között akkora szakadékok húzódnak, hogy a keresztalkalmazhatóság egyáltalán nem magától értetődő.
Példaként tekintsük az esélyesek között számon tartott HIV-ellenes szereket – ehhez azonban előbb gyorsan fussunk át a HIV életciklusán. A HIV retrovírus, tehát a gazdasejtbe jutva egyszálú RNS-ből álló örökítőanyagát először kétszálú DNS-re másolja, majd ezt a DNS-darabot beilleszti a gazdasejt genomjába.
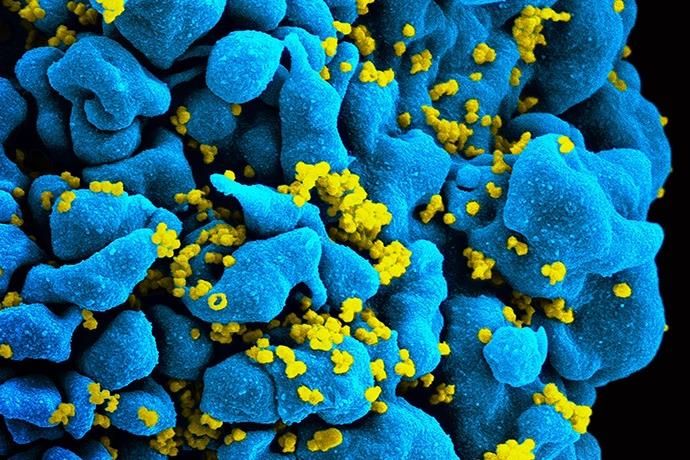
A vírus-örökítőanyag itt évekig észrevétlenül megbújik,
mígnem egyszer csak aktiválódik, és elkezd átíródni, amikor is a DNS-ről újra egyszálú RNS-másolatok készülnek. Ezek a vírus-RNS-ek a vírusfehérjék legyártására kényszerítik a sejtet, majd belecsomagolódnak a fehérjékbe, és új vírusrészecskéket hoznak létre, amelyek a sejtből kijutva továbbviszik a fertőzést.
A HIV-ellenes gyógyszerek három fő csoportja közül a nukleozid-analógok az RNS-ről DNS-re másoló virális enzimet, a reverz transzkriptázt (RT-t) gátolják, míg az integrázgátlók a víruseredetű DNS gazdagenomba illesztését, a proteázgátlók pedig a vírus ún. poliproteinjének (több fehérjéből álló füzérének) egyedi fehérjékre való feldarabolását akadályozzák.
A COVID-19 örökítőanyaga szintén egyszálú RNS, de ő erről nem készít DNS-másolatot, tehát RT-je sincs.
Szerencsére van viszont RNS-függő RNS-polimeráza, amivel a genomját másolja, és ez az enzim szintén gátolható az RT-re szabott nukleozid-analógok némelyikével.
Úgyszintén van proteáza, amivel a maga poliproteinjét hasogatja, s a jelek szerint legalábbis néhány HIV-proteázgátló hatásos lehet a COVID-19 proteázával szemben.
Az integrázgátlók ellenben a HIV életciklusának egy olyan lépését – a gazdagenomba illesztést – gátolják, amely a COVID-19 életciklusában nem szerepel, így ezek a szerek eleve kiesnek a versenyből.
A HIV-ellenes szerek mellett egyéb antivirális szerek, így a más RNS- ellen kifejlesztett nukleobázis-, nukleozid- és nukleotid-analógok is eredményesek lehetnek a COVID-19-cel szemben.
Kiemelendő közülük az eredetileg az Ebola- és a Marburg-vírusok RNS-replikációjának gátlására szánt nukleotid-analóg, a remdesivir, amelynek széles hatásspektruma már egy sor egyszálú RNS-vírus, köztük a SARS és a MERS koronavírusa esetében igazolódott.
Érdekes módon az eredetileg teljesen más alkalmazási körű,
elsődlegesen maláriaellenes szerként ismert klorokin és hidroxiklorokin neve is felmerült a lehetséges COVID-19-ellenes gyógyszerek között.
A klorokin és származékai akadályozzák a vírus életciklusának azt a lépését, melyben a gazdasejtbe jutott, de még sejthártyával körülhatárolt vírus kiszabadul az őt akadályozó burokból.
Végezetül egy záró spekuláció erejéig röviden elidőzhetünk annál a kérdésnél, hogy a COVID-19 változékonysága vajon a mostaninál gyilkosabb vagy enyhébb variánsokkal fogja meglepni az emberiséget.
Ezzel kapcsolatban visszautalhatunk arra a gondolatra, hogy a parazitáknak alapvetően nem céljuk a gazda pusztulása, és vírusból sem a leggyilkosabb lesz a legsikeresebb.

Egy olyan vírus, amely súlyosan megbetegíti, sőt, esetleg megöli áldozatát, mielőtt az sok további gazdának átadhatta volna a fertőzést,
valószínűleg nem fog jelentős járványt okozni
– különösen, ha a nyilvánvalóan beteg, súlyos tüneteket mutató fertőzötteket azonnal elkülönítik. Egy olyan vírus ellenben, amellyel vígan járunk-kelünk, és észre sem vesszük a jelenlétét, akadálytalanul terjedhet egészen addig, amíg a teljes emberiséget át nem fertőzte.
A COVID-19 egyelőre ügyesen lavíroz: tünetmentes lappangási ideje, mely alatt már fertőz, illetve a mindvégig tünetmentesen lezajló fertőzések magas aránya biztosítja a hatékony terjedését.
Épp azért szükségesek a mindenkire kiterjedő érintkezéskorlátozó intézkedések, mert a terjesztés zömét tünetmentes hordozók végzik.
A 2002-03-as SARS-járvány esetében a tünetek azelőtt jelentkeztek, hogy a betegek érdemben terjeszteni kezdték volna a vírust, ezért gyorsan és hatékonyan izolálni lehetett őket.
A súlyosabb lefolyás – ami magasabb halálozási aránnyal is járt – nem kedvezett tehát a járvány pandémiává terebélyesedésének, amely így 8 hónap alatt, összesen 8098 fertőzött és 774 haláleset után véget ért.
Mivel a két vírus ettől eltekintve sok hasonló jellemzővel bír, talán észszerű azt remélni, hogy ha kialakulnak is a COVID-19 gyilkosabb változatai, azok nem fogják átvenni a vezetést a most uralkodó variáns előtt.










